줄기세포 치료제 언제쯤 나올까
매일경제 | 입력 2011.03.09 17:05
" '제2 황우석 사태'가 생기는 것은 막아야 한다." 애초 지난해 말 승인될 것으로 예상했던 에프씨비파미셀의 줄기세포 치료제(급성심근경색 치료)가 승인에 진통을 겪고 있다.
노연홍 식품의약품안전청장은 이와 관련해 "줄기세포 치료제가 향후 성장동력이 될 수 있다는 기대감에 세계 첫 줄기세포 치료제 인가에 대한 사회적 압박이 심하다"면서 "그러나 향후 국제학회에서 쏟아질 질문에 막힘없이 대응할 수 있도록 전문가들이 모여 회의를 하면서 검증을 철저히 하고 있다"고 말했다.
그는 이어 "세계 최초로 줄기세포 치료제를 인정하는 것은 일반 의약품 허가를 내주는 것보다 몇 배는 더 부담되는 일"이라고 고충을 토로했다.
줄기세포 치료제는 세계적으로도 인가를 받은 전례가 없어 식약청이 허가심사 지침 등 벤치마킹할 자료 때문에 애를 태우고 있다. 특히 줄기세포 치료제에 특화한 허가심사를 위한 지침으로는 유럽의약품청(EMA)이 지난해 3월 마련한 11쪽 분량의 자료가 유일한데 줄기세포 주입에 따른 종양 발생 위험, 목표 부위가 아닌 곳의 분화 여부 등을 장기간 확인하도록 권고하는 내용이 담겨 있는 것으로 알려졌다.
식약청이 장고에 들어가면서 에프씨비파미셀의 줄기세포 치료제의 이달 인가 가능성이 확실하지 않은 상황이다.
에프씨비파미셀은 지난해 12월 급성심근경색 치료제의 품목허가를 받는 데 필요한 기준 및 시험 방법, GMP(우수의약품제조관리기준) 자료와 안전성ㆍ유효성 허가 자료 등 3건에 대한 허가심사 신청을 모두 완료했다. 식약청은 이 회사가 제출한 시험 방법, 안전성과 유효성 허가 자료에 대해 보완을 요청했으며 회사는 보완 기간인 60일에 대해 연장을 다시 요청했다.
유무영 식약청 대변인은 "미국 식품의약국(FDA)이나 EMA에서 품목허가를 심사 중인 줄기세포 치료제는 아직 없는 것으로 알고 있다"고 말했다.
이와 함께 메디포스트도 관절연골재생 치료제의 최종 임상시험을 마치고 품목허가 승인을 위한 자료를 최근 식약청에 제출해 첫 줄기세포 치료제를 놓고 에프씨비파미셀과 경쟁할 것으로 보인다.
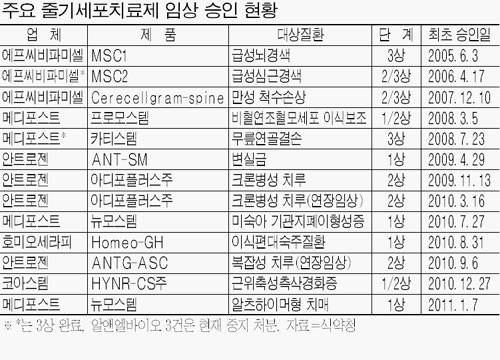
식약청에 따르면 줄기세포 임상시험을 허가받은 것은 모두 20건에 달한다. 익명을 요구한 한 줄기세포 전문가는 "줄기세포가 만능치료제라고 알려지면서 기대가 크지만 실제 치료제가 나와도 대박을 터뜨리는 것은 아니라는 것을 명심해야 한다"고 말했다.
의약품으로 줄기세포 치료제는 난항을 겪고 있지만 줄기세포 기술을 이용한 화장품이나 세포치료제로 성과를 올리고 있는 기업도 있다.
일본에서 1회 시술에 10만엔(약 130만원)하는 고가 피부재생시술에 사용되는 화장품은 한국 바이오기업인 프로스테믹스 제품이다. 이 회사가 개발한 지방줄기세포 화장품 원료가 일본 도쿄를 중심으로 한 200여 곳 피부과ㆍ성형외과에서 사용되고 있다. 줄기세포가 다양한 재생능력을 발휘하는 것은 줄기세포가 만들어내는 단백질의 효과 때문인데 이를 토대로 상업화(제품화)한 것이다.
프로스테믹스는 2006년 지방줄기세포 배양액에서 추출한 단백질 원료를 세계 최초로 미국 화장품협회(PCPC)에 'AAPE'라는 이름으로 원료 등재했으며 관련 기술을 특허 등록했다.
일본에는 2008년 진출했으며 피부와 모근 재생을 위주로 병ㆍ의원에서 사용되고 있다. 프로스테믹스의 지난해 일본 수출액은 100만달러에 달한다.
이원종 프로스테믹스 사장은 "피부과ㆍ성형외과 등에서 광범위하게 사용되는 레이저 치료 이후 이 제품을 적용할 경우 피부 회복과 개선 속도가 두 배 가까이 빨라진다"고 말했다.
안트로젠은 2007년 식약청에서 줄기세포를 이용한 주름치료제를 세포치료제로 품목허가 받았다. 이어 일본 제약사인 니혼파마와 총 400만달러 규모 기술수출 계약을 맺었다.
[박기효 기자 / 이유진 기자]
노연홍 식품의약품안전청장은 이와 관련해 "줄기세포 치료제가 향후 성장동력이 될 수 있다는 기대감에 세계 첫 줄기세포 치료제 인가에 대한 사회적 압박이 심하다"면서 "그러나 향후 국제학회에서 쏟아질 질문에 막힘없이 대응할 수 있도록 전문가들이 모여 회의를 하면서 검증을 철저히 하고 있다"고 말했다.
줄기세포 치료제는 세계적으로도 인가를 받은 전례가 없어 식약청이 허가심사 지침 등 벤치마킹할 자료 때문에 애를 태우고 있다. 특히 줄기세포 치료제에 특화한 허가심사를 위한 지침으로는 유럽의약품청(EMA)이 지난해 3월 마련한 11쪽 분량의 자료가 유일한데 줄기세포 주입에 따른 종양 발생 위험, 목표 부위가 아닌 곳의 분화 여부 등을 장기간 확인하도록 권고하는 내용이 담겨 있는 것으로 알려졌다.
식약청이 장고에 들어가면서 에프씨비파미셀의 줄기세포 치료제의 이달 인가 가능성이 확실하지 않은 상황이다.
에프씨비파미셀은 지난해 12월 급성심근경색 치료제의 품목허가를 받는 데 필요한 기준 및 시험 방법, GMP(우수의약품제조관리기준) 자료와 안전성ㆍ유효성 허가 자료 등 3건에 대한 허가심사 신청을 모두 완료했다. 식약청은 이 회사가 제출한 시험 방법, 안전성과 유효성 허가 자료에 대해 보완을 요청했으며 회사는 보완 기간인 60일에 대해 연장을 다시 요청했다.
유무영 식약청 대변인은 "미국 식품의약국(FDA)이나 EMA에서 품목허가를 심사 중인 줄기세포 치료제는 아직 없는 것으로 알고 있다"고 말했다.
이와 함께 메디포스트도 관절연골재생 치료제의 최종 임상시험을 마치고 품목허가 승인을 위한 자료를 최근 식약청에 제출해 첫 줄기세포 치료제를 놓고 에프씨비파미셀과 경쟁할 것으로 보인다.
식약청에 따르면 줄기세포 임상시험을 허가받은 것은 모두 20건에 달한다. 익명을 요구한 한 줄기세포 전문가는 "줄기세포가 만능치료제라고 알려지면서 기대가 크지만 실제 치료제가 나와도 대박을 터뜨리는 것은 아니라는 것을 명심해야 한다"고 말했다.
의약품으로 줄기세포 치료제는 난항을 겪고 있지만 줄기세포 기술을 이용한 화장품이나 세포치료제로 성과를 올리고 있는 기업도 있다.
일본에서 1회 시술에 10만엔(약 130만원)하는 고가 피부재생시술에 사용되는 화장품은 한국 바이오기업인 프로스테믹스 제품이다. 이 회사가 개발한 지방줄기세포 화장품 원료가 일본 도쿄를 중심으로 한 200여 곳 피부과ㆍ성형외과에서 사용되고 있다. 줄기세포가 다양한 재생능력을 발휘하는 것은 줄기세포가 만들어내는 단백질의 효과 때문인데 이를 토대로 상업화(제품화)한 것이다.
프로스테믹스는 2006년 지방줄기세포 배양액에서 추출한 단백질 원료를 세계 최초로 미국 화장품협회(PCPC)에 'AAPE'라는 이름으로 원료 등재했으며 관련 기술을 특허 등록했다.
일본에는 2008년 진출했으며 피부와 모근 재생을 위주로 병ㆍ의원에서 사용되고 있다. 프로스테믹스의 지난해 일본 수출액은 100만달러에 달한다.
이원종 프로스테믹스 사장은 "피부과ㆍ성형외과 등에서 광범위하게 사용되는 레이저 치료 이후 이 제품을 적용할 경우 피부 회복과 개선 속도가 두 배 가까이 빨라진다"고 말했다.
안트로젠은 2007년 식약청에서 줄기세포를 이용한 주름치료제를 세포치료제로 품목허가 받았다. 이어 일본 제약사인 니혼파마와 총 400만달러 규모 기술수출 계약을 맺었다.
[박기효 기자 / 이유진 기자]